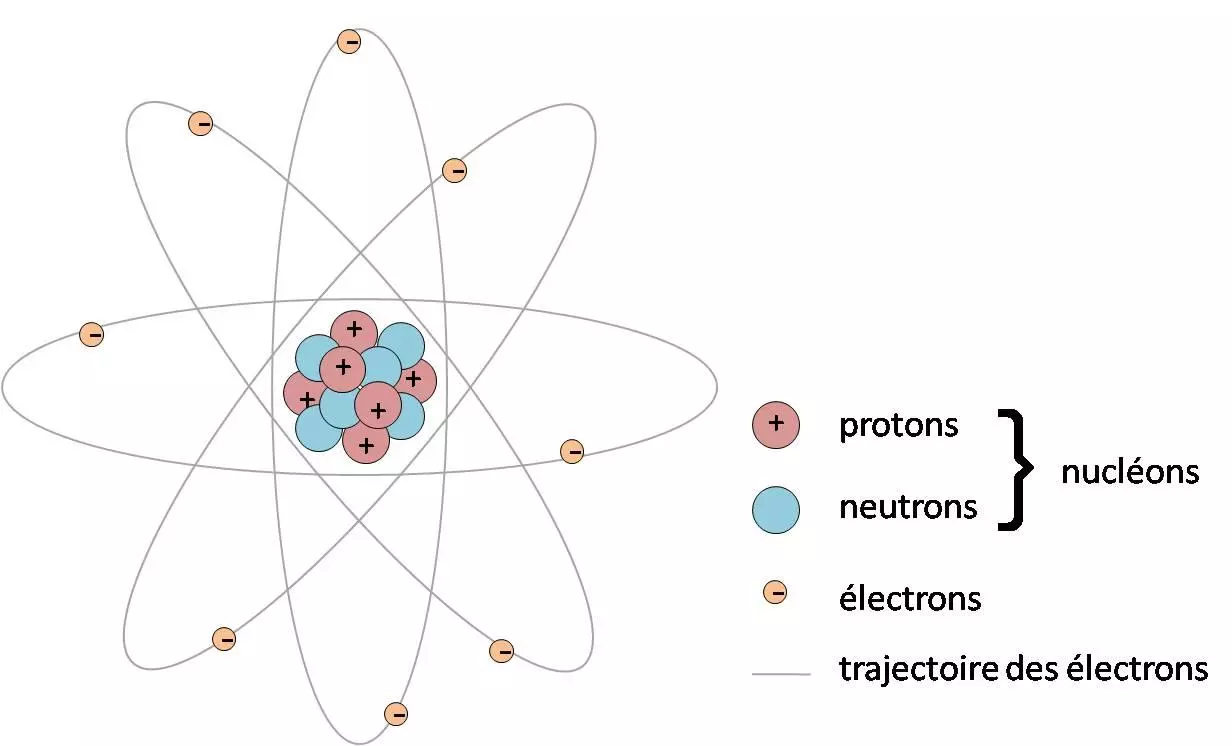
L’atome est la plus petite unité de matière qui conserve les propriétés chimiques d’un élément. Il est constitué d’un noyau central chargé positivement autour duquel évoluent des électrons chargés négativement.
Découverte de l’atome
L’atome a été imaginé pour la première fois par le scientifique grec Démocrite au 5ème siècle avant JC. Démocrite a postulé que la matière était composée d’unités indivisibles qu’il a appelées « atomes ».
Au cours des siècles suivants, de nombreux scientifiques ont étudié la nature de l’atome. En 1803, John Dalton a proposé un modèle atomique simple dans lequel les atomes sont des sphères indivisibles de matière.
En 1897, Joseph Thomson a découvert l’électron, une particule chargée négativement. Cela a conduit à la conclusion que les atomes sont constitués d’un noyau positif entouré d’électrons négatifs.
En 1911, Ernest Rutherford a réalisé une expérience qui a montré que le noyau de l’atome était très petit et dense. Il a également découvert que le noyau était constitué de protons, des particules chargées positivement, et de neutrons, des particules non chargées (neutre électriquement).
Description de l’atome
Un atome est composé de trois types de particules :
- Les protons sont des particules chargées positivement. Ils se trouvent dans le noyau de l’atome.

- Les neutrons sont des particules non chargées. Ils se trouvent aussi dans le noyau de l’atome.
- Les électrons sont des particules chargées négativement. Ils évoluent autour du noyau de l’atome.

Le nombre de protons dans le noyau d’un atome est appelé son nombre atomique ou nombre de charges, noté Z. Le nombre atomique est unique pour chaque élément chimique. Un atome étant électriquement neutre, il correspond, aussi, au nombre d’électrons.
Le nombre de neutrons, noté N, dans le noyau d’un atome peut varier. Les atomes d’un même élément chimique avec un nombre différent de neutrons sont appelés isotopes.
Le nombre de protons et de neutron, noté A=Z+N, constitue le nombre de masse. Cet ensemble de particule est responsable de la masse de l’atome.
Les ions
Un ion est un atome ou un groupe d’atomes qui a perdu ou gagné des électrons. Les ions sont chargés électriquement, ce qui les rend différents des atomes qui,, eux, sont neutres.
Les ions positifs, également appelés cations, ont perdu des électrons. Ils ont donc un excès de protons, ce qui leur confère une charge positive.
Les ions négatifs, aussi appelés anions, ont gagné des électrons. Ils ont donc un excès d’électrons, ce qui leur confère une charge négative.
Les ions sont importants en chimie, car ils sont impliqués dans de nombreuses réactions chimiques. Ils sont, de plus, importants dans la vie quotidienne, puisqu’ils sont présents dans de nombreux matériaux, tels que les sels, les acides et les bases.
Exemples d’ions
- Le sodium (Na) est un élément chimique qui a un nombre atomique de 11. Il a donc 11 protons dans son noyau et 11 électrons autour de son noyau.
- Lorsque le sodium perd un électron, il devient un ion sodium (Na+). Le sodium a donc 11 protons et 10 électrons. Il a donc un excès de protons, ce qui le rend chargé positivement.
- Le chlore (Cl) est un autre élément chimique qui a un nombre atomique de 17. Il a donc 17 protons dans son noyau et 17 électrons autour de son noyau.
- Lorsque le chlore gagne un électron, il devient un ion chlorure (Cl–). Le chlore a donc 17 protons et 18 électrons. Il a donc un excès d’électrons, ce qui le rend chargé négativement.
La mole
La mole est une unité de mesure utilisée en chimie pour mesurer la quantité de matière. Une mole d’une substance contient un nombre d’entités égal au nombre d’Avogadro. La constante d’Avogadro est égale à 6,02.1023 entités.
Par exemple, 12g de carbone-12 (612C) contienent 1mol de carbone.
L’isotopie
L’isotopie est un phénomène qui se produit lorsque les atomes d’un même élément chimique ont un nombre différent de neutrons. Les isotopes d’un élément chimique ont le même nombre de protons, mais un nombre différent de neutrons.
Les isotopes d’un élément chimique peuvent avoir des propriétés physiques et chimiques différentes. Par exemple, les isotopes de l’hydrogène ont des masses différentes. L’hydrogène-1, le plus abondant des isotopes de l’hydrogène, a une masse de 1,00784 u. L’hydrogène-2, également connu sous le nom de deutérium, a une masse de 2,01410 u. L’hydrogène-3, par ailleurs connu sous le nom de tritium, a une masse de 3,01605 u.
L’isotopie est un phénomène important en chimie et en physique. Elle est utilisée dans de nombreuses applications, notamment la datation au carbone, la médecine nucléaire et la recherche nucléaire.
L’unité de masse atomique unifiée, de symbole « u », est une unité de mesure utilisée pour exprimer la masse des atomes. Cette unité n’appartient pas au SI, mais son usage est accepté.
1 u=1,66.10−24 g
Conclusion
L’atome est la plus petite unité de matière qui conserve les propriétés chimiques d’un élément. Il est constitué d’un noyau central chargé positivement autour duquel évoluent des électrons chargés négativement.
Les atomes d’un même élément chimique peuvent avoir un nombre différent de neutrons. Ces atomes sont appelés isotopes. Les isotopes d’un élément chimique peuvent avoir des propriétés physiques différentes.
La mole est une unité de mesure utilisée en chimie pour mesurer la quantité de matière.